Fordította: Dr. Kurnát Rita
A homeopátiás kezelés, mint kiegészítő terápia javíthatja az életminőséget és hosszabb túlélést jelenthet a nem kissejtes tüdődaganatban (NSCLC) szenvedő betegek esetében- egy prospektív, randomizált, placebo-kontrollos, kettős-vak, három-karos, multicentrikus vizsgálat szerint
- Háttér:
Az előrehaladott, nem kissejtes tüdődaganatban (NSCLC) szenvedő betegek kezelési lehetőségei korlátozottak. A hagyományos daganatellenes kezelés mellett a homeopátia, mint kiegészítő gyógymód segítséget jelenthet a konvencionális terápia mellékhatásainak csökkentésében. E tanulmány célja, hogy vizsgálja a homeopátiás kiegészítő kezelés hatását az életminőségre (QoL) és túlélésre, a nem kissejtes tüdődaganatban (NSCLC) szenvedő betegeknél.
- Módszer:
Ebben a prospektív, randomizált, placebo-kontrollos, kettős-vak, három-karú, multicentrikus, III. fázisú vizsgálatban a kiegészítő homeopátiás kezelés hatásait értékeltük a placebo hatással összevetve IV stádiumú NSCLC-ben szenvedő betegeknél, mindkét, véletlenszerűen besorolt csoportban vizsgálva az életminőségre gyakorolt hatást és mindhárom csoportban vizsgálva a túlélési időt. A kezelt betegek 9 hetente keresték fel a járóbeteg-rendelést: 150 IV stádiumú NSCLC-ben szenvedő beteget vontak be a vizsgálatba, 98 beteg kapott vagy individualizált homeopátiás gyógyszert (51 beteg), vagy placebot (47 beteg), kettős-vak kiválasztással, és a kontrollcsoportban résztvevő, homeopátiás kiegészítésben nem részesülő 52 betegnél csak a túlélési idő hosszát vizsgálták. A különböző homeopátiás gyógyszereket nagyrészt ásványi, növényi vagy állati eredetű szerek alkották. A gyógyszereket lépésenkénti higítással és ütverázással (dinamizálással) állították elő, ezáltal megfelelve a GMP által támasztott gyógyszerformuláció előírásainak.
- Eredmények:
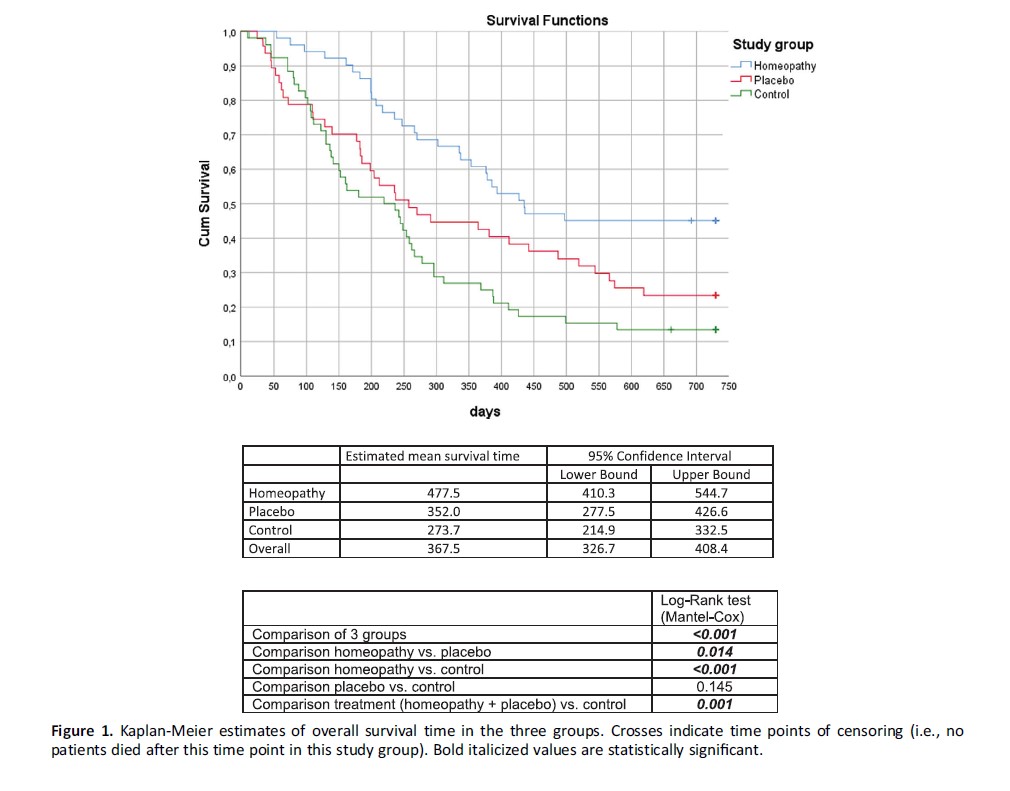
Az életminőség (QoL), valamint a funkcionális és tüneti skálák szignifikáns javulást mutattak a homeopátiás csoportban, a placeboval összehasonlítva, 9 és 18 hét homeopátiás kezelés után (p <.001). Az átlagos túlélési idő szignifikánsan volt hosszabb a homeopátiás csoportban (435 nap), szemben a placeboval (257 nap; p = 0,10), valamint a kontrollcsoporthoz képest is (228 nap; p <.001). A túlélési arány a homeopátiás csoportban szignifikánsan eltért a placebo - (p = 0,020) és a kontrollcsoportnál tapasztalhatótól (p <0,001).
- Következtetés:
Az életminőség jelentősen javult a homeopátiát is kapók csoportjában, a placebocsoporttal összehasonlítva. Ezen túlmenően a túlélés volt szignifikánsan hosszabb a homeopátiás csoportban, a placebo- és kontrollcsoporthoz képest. A magasabb életminőség (QoL) hozzájárulhatott a hosszabb távú túléléshez. A tanulmány azt mutatja, hogy a homeopátia nemcsak a QoL-t, hanem a túlélést is pozitívan befolyásolja. Érdemes további vizsgálatokat folytatni, akár más daganatos megbetegedésekre vonatkozóan is. The Oncologist 2020; 25: 1–26
- Megbeszélés:
Hasonlóan a korábbi nyílt, véletlen besorolású klinikai vizsgálatunkhoz [19], a jelenlegi, véletlen besorolású (randomizált), placebo-kontrollos, kettős-vak vizsgálatunkban a kiegészítő homeopátiás kezelés szignifikánsan javította a daganatos betegek általános egészségi állapotát, a közérzetüket saját szubjektív megítélésük szerint is, illetve javult számos funkció és tüneti skála, az EORTC (A daganatos betegségek kezelésének és kutatásának európai szervezete), illetve egy 36 pontos egészségügyi kérdőívnek megfelelő értékelésben [24, 25].
Előre nem várt módon, a homeopátiás kezeléssel a túlélés idő is megemelkedett. Az átlagos túlélési idő a homeopátiát kapók csoportjában 6 hónappal hosszabb volt, mint a placebo csoportban és 7 hónappal hosszabb, mint a kontroll csoport esetében. Az átlagos túlélési idő a placebo csoportban körülbelül 8,5 hónap volt, a szakirodalmi adatokhoz közelítően. Továbbá, az átlagos túlélési idő azoknál a betegeknél, akik az esetkövetési/ megfigyelési időszakban haltak meg, szignifikánsan hosszabb volt a homeopátiát kapók csoportjában (8,4 hónap), mint a placebo csoportban (6,4 hónap), illetve a kontroll csoportban (5,2 hónap). Az általános túlélési idő a meghatározás szerint a véletlenszerű kiválasztástól számított 2 év, vagy az ennél korábban bekövetkező elhalálozásig tartó időszak. A halálozási adatokat a független Information Technology Solution Center (ITSC), Austria szolgáltatta, és az adatok rögzítését olyan személy végezte, aki nem vett részt a vizsgálatban. (E.E.)
A homeopátiás kezelésben is részesülő csoportban valamivel több volt a laphámsejtes karcinómával kezelt beteg, bár ez a különbség nem volt szignifikáns. Mivel a laphámsejtes karcinóma prognózisa rosszabb, mint az adenokarcinómáé, a vizsgálat eredményeit ez még inkább igazolhatja.
Tanulmányunkban a túlélési időre vonatkozó különbség a placebo- és kontrollcsoport között összhangban van a Temel és munkatársai által közölt eredményekkel [28]. Temel azt vizsgálta, hogy a nem sokkal a diagnózist követően bevezetett palliatív gondozás milyen hatással van a betegek által jelentett eredményekre, illetve vizsgálta az újonnan diagnosztizált, ambuláns betegek életvégi gondozását. Az újonnan diagnosztizált, áttétes, nem kissejtes tüdőrák (NSCLC) –ban szenvedő betegek véletlenszerű kiválasztással kaptak korai palliatív gondozást a protokoll szerinti (standard) onkológiai kezelés mellett vagy pedig csak standard kezelésben részesültek. Annak ellenére, hogy a palliatív gondozást is kapó csoportban kevesebb beteg részesült agresszív életvégi terápiában a csak standard onkológiai kezelést kapó csoporthoz képest (33% vö. 54%, p = .05), az átlagos túlélés hosszabb volt a korai palliatív gondozásban is részesülő betegek körében (11.6 hónap vö. 8.9 hónap, p = .02). A szerzők arra a következtetésre jutottak, hogy az áttétes, nem kissejtes tüdőrák (NSCLC) –ban szenvedő betegeknél bevezetett korai támogató kezelés (palliatív gondozás) jelentős javuláshoz vezetett mind az életminőség, mind a hangulat tekintetében. A standard kezeléssel összehasonlítva a korai palliatív gondozást kapó betegek kevesebb agresszív kezelésben (beavatkozásban) részesültek életük végén, mégis hosszabb túlélési idő jellemezte őket l [28].
Deng és munkatársai arról számoltak be, hogy a daganatos betegek gyakran érdeklődnek kezelőorvosuknál a kiegészítő terápiás lehetőségekről és az adatok azt mutatják, hogy mind az érdeklődés, mind a komplementer kezelés igénybevétele gyakori a daganatos betegségben szenvedőknél n [29].. Ezért nagy jelentőségű a komplementer terápiák előnyeinek és kockázatainak értékelése a már rendelkezésre álló (jelenlegi, meglévő) bizonyítékok alapján. Számos kiegészítő terápiás módszer hasznos lehet a tüdődaganatos betegek általános állapotának javításában. A placebo-hatások úgy tűnik, kisebb jelentőséggel bírnak, a homeopátia a kritikus állapotú betegeknél is működik [30].
A cikkben szereplő vizsgálatra visszatérve az életminőség, akárcsak a funkcionális és tüneti skála szignifikáns javulást mutatott a homeopátiás csoportban a placebo csoporthoz képest a 9 és 18 hetes homeopátiás kezelést követően. Továbbá az eredmények szerint a homeopátiás kiegészítő kezelés az általános túlélési esélyeket is javította az előrehaladott NSCLC-ben szenvedő betegeknél azáltal, hogy szignifikánsan csökkentette a 2 éven belüli halálozást a kontrollcsoportnál jellemző 86,5%-ról; a placebocsoportnál a halálozás 76, 6%-ra csökkent, míg a homeopátiát kapó betegek csoportjánál 54,9%-ra. A becsült medián (átlagos) túlélési idő szignifikánsan hosszabb volt a homeopátiát kapó betegek csoportjánál. Ezek az eredmények egybeesnek azzal az előzetesen jelentett közelítőleg 50%-os kockázattal, amely a betegség előrehaladására és a (lehetséges) halálozásra vonatkozik.
A beavatkozásban nem részesülő kontrollcsoport bevonásával lehetségessé vált a valós homeopátiás hatások felmérése a homeopátiás csoportban, mert így látható az a valódi hatás, amit a betegség természetes lefolyására gyakorol a homeopátia illetve a placebo.
A vizsgálati időszak viszonylagos hosszúsága egyben korlátot is jelentett. Mindazonáltal, a teljes vizsgálati időszak alatt a konvencionális alapterápia (hagyományos bázisterápia) lényegében változatlan maradt. További korlátozó tényező, hogy a hagyományos terápia ebben a vizsgálatban a napjainkban használatos immuno-onkológiai terápiák nélkül zajlott majdnem minden beteg esetében [31], mivel a vizsgálat 2015 előtt kezdődött. Habár az EGFR/ALK tirozin-kináz inhibitorok standard első vonalbeli kezelési stratégiává váltak az előrehaladott állapotú, EGFR-mutáció pozitív vagy ALK-fúziós onkogén pozitív NSCLC betegségben szenvedőknél, és javították a gyógyulási esélyt, a mutáció nélküli NSCLC-ben szenvedő kontrollcsoporthoz tartozó betegek standard terápiája csak konvencionális kemoterápiából állt a vizsgálat során. Olyan immunmoduláló gyógyszerek jóváhagyása/engedélyezése, melyek bizonyos ponton gátló hatást fejtenek ki, mint a nivolumab, pembrolizumab, atezolizumab, és amelyeket második vonalbeli kezelésként alkalmaznak a nem kissejtes tüdődaganatok (NSCLC) kezelésénél a platina bázisú terápia sikertelensége esetén a CheckMate 017, CheckMate 057, KEYNOTE 010, and OAK vizsgálatok alapján, befolyásolhatták az általános túlélés analízist ennél a vizsgálatnál. Mindazonáltal ez a feltételezett torzító hatás nem releváns, mivel a későbbi immun-onkológiai terápiával kezelt betegek száma hasonló volt (p = .942) az egyes csoportok között (Table 1).
Ma az immun-onkológiai kezelés és a kemoterápia elsőként választandó terápia. Ezért további vizsgálatok szükségesek, melyekben az immun-onkológiai kezelés is szerepet kap, hogy tanulmányozhassák a homeopátiás terápia hatásait a (daganatellenes) terápiák modern formáival együtt.
A homeopátiás kiegészítő terápia gyógyszereinek költségei nagyon alacsonyak az immun-onkológiai készítményekkel összehasonlítva. Tehát a daganatellenes kezelés költségeinek összefüggésében a homeopátiás kezelés járulékos költségei elhanyagolhatóan alacsonyak. Módszertani szempontokból nézve a kiegészítő homeopátiás kezelés bármely más konvencionális terápiával összeférhető. Tehát a homeopátiás kiegészítő kezelés számos előnnyel rendelkezik: összeférhető (nem ad interakciót) más kezelési módokkal, nem terheli a betegek szervezetét /anyagcseréjét és költségei alacsonyak.
Irodalomjegyzék:
- 1. Cancer facts and statistics. American Cancer Society Web site. 2016. http://www.cancer.org/ research/cancerfactsstatistics/index. Accessed February 22, 2017.
- 2. Jemal A, Siegel R, Xu J et al. Cancer statistics. CA Cancer J Clin 2010;60:277–300.
- 3. Molina JR, Yang P, Cassivi SD et al. Non-small cell lung cancer: Epidemiology risk factors, treatment, and survivorship. Mayo Clin Proc 2008;83: 584–594.
- 4. Hirsch FR, Scagliotti GV, Mulshine JL et al. Lung cancer: Current therapies and new targeted treatments. Lancet 2017;389:299–311.
- 5. Ettinger DS, Wood DE, Aisner DL et al. Nonsmall cell lung cancer, version 2017, NCCN clinical practice guidelines in oncology. J Natl Compr Cancer Netw 2017;15:504–535.
- 6. Shojaee S, Nana-Sinkam P. Recent advances in the management of non-small cell lung cancer. F1000Res 2017;6:2110.
- 7. Tanaka K, Akechi T, Okuyama T et al. Impact of dyspnea, pain, and fatigue on daily life activities in ambulatory patients with advanced lung cancer. J Pain Symptom Manag 2002;23:417–423.
- 8. Iyer S, Taylor-Stokes G, Roughley A. Symptom burden and quality of life in advanced non-small cell lung cancer patients in France and Germany. Lung Cancer 2013;81:288–293.
- 9. Iyer S, Roughley A, Rider A et al. The symptom burden of non-small cell lung cancer in the USA: A real-world cross-sectional study. Support Care Cancer 2014;22:181–187.
- 10. Temel JS, Pirl WF, Lynch TJ. Comprehensive symptom management in patients with advanced-stage non-small-cell lung cancer. Clin Lung Cancer 2006;7:241–249.
- 11. Cooley ME. Symptoms in adults with lung cancer. A systematic research review. J Pain Symptom Manag 2000;19:137–153.
- 12. Akin S, Can G, Aydiner A et al. Quality of life, symptom experience and distress of lung cancer patients undergoing chemotherapy. Eur J Oncol Nurs 2010;14:400–409.
- 13. Cella D, Peterman A, Hudgens S et al. Measuring the side effects of taxane therapy in oncology: The functional assessment of cancer therapy-taxane (FACT-taxane). Cancer 2003;98:
- 822–831.
- 14. Sloan JA, Zhao X, Novotny PJ et al. Relationship between deficits in overall quality of life and non-small-cell lung cancer survival. J Clin Oncol 2012;30;1498–1504.
- 15. Wang XS, Shi Q, Lu C et al. Prognostic value of symptom burden for overall survival in patients receiving chemotherapy for advanced non-small cell lung cancer. Cancer 2010;116:137–145.
- 16. Daly BJ, Douglas SL, Foley H. Psychosocial registry for persons with cancer: A method of facilitating quality of life and symptom research. Psychooncology 2007;16:358–364.
- 17. Hahnemann S. Organon of Medicine. 6th ed. New Delhi, India: B. Jain Publishers Ltd., 1994.
- 18. Kent JT. Lectures on Homoeopathic Philosophy. New Delhi, India: B. Jain Publishers Ltd., 1993; 92–93.
- 19. Frass M, Friehs H, Thallinger C et al. Influence of adjunctive classical homeopathy on global health status and subjective wellbeing in cancer patients - A pragmatic randomized controlled trial. Complement Ther Med 2015;23:309–317.
- 20. Gleiss A, Frass M, Gaertner K. Re-analysis of survival data of cancer patients utilizing additive homeopathy. Complement Ther Med 2016;27: 65–67.
- 21. Brien S, Lachance L, Prescott P et al. Homeopathy has clinical benefits in rheumatoid arthritis patients that are attributable to the consultation process but not the homeopathic remedy: A randomized controlled clinical trial. Rheumatology (Oxford) 2011;50:1070–1082.
- 22. Scagliotti GV, Parikh P, von Pawel J et al. Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advanced stage non-small-cell lung cancer. J Clin Oncol 2008;26:3543–3551.
- 23. Muchitsch I. Remedy production and quality, Potentisation. In: Frass M, Bündner M, eds. Homeopathy in Intensive and Emergency Medicine. Kandern, Germany: Narayana Verlag, 2015:37–55.
- 24. Fayers P, Bottomley A; EORTC Quality of Life Group; Quality of Life Unit. Quality of life research within the EORTC-the EORTC QLQ-C30. European Organisation for Research and Treatment of Cancer. Eur J Cancer 2002;38(suppl 4): 25–133.
- 25. Hays RD, Sherbourne CD, Mazel RM. The RAND 36-item health survey 1.0. Health Econ 1993;2:17–227.
- 26. Pirker R, Pereira JR, Szczesna A et al.; FLEX Study Team. Cetuximab plus chemotherapy in patients with advanced non-small-cell lung cancer (FLEX): An open-label randomised phase III trial. Lancet 2009;373:1525–1531.
- 27. Kawase A, Yoshida J, Ishii G et al. Differences between squamous cell carcinoma and adenocarcinoma of the lung: Are adenocarcinoma and squamous cell carcinoma prognostically equal? Jpn J Clin Oncol 2012;42: 189–195.
- 28. Temel JS, Greer JA, Muzikansky A et al. Early palliative care for patients with metastatic nonsmall- cell lung cancer. N Engl J Med 2010;363:733–742.
- 29. Deng GE, Rausch SM, Jones LW et al. Complementary therapies and integrative medicine in lung cancer: Diagnosis and management of lung cancer, 3rd ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest 2013;143(suppl 5):e420S–e436S.
- 30. Frass M, Dielacher C, Linkesch M et al. Influence of potassium dichromate on tracheal secretions in critically ill patients. Chest 2005;127: 936–941.
- 31. Gandhi L, Rodríguez-Abreu D, Gadgeel S et al. Pembrolizumab plus chemotherapy in metastatic non-small-cell lung cancer. N Engl J Med 2018;378:2078–2092.
- 32. Montazeri A. Quality of life data as prognostic indicators of survival in cancer patients: An overview of the literature from 1982 to 2008. Health Qual Life Outcomes 2009;7:102.
-
33. Lu W, Giobbie-Hurder A, Freedman RA et al. Acupuncture for chemotherapy-induced peripheral neuropathy in breast cancer survivors: A randomized controlled pilot trial. The Oncologist 2020;25:310–318.
Michael Frass,a Peter Lechleitner,b Christa Gründling,c Claudia Pirker,d Erwin Grasmuk-Siegl,d Julian Domayer,d,Maximilian Hochmair,d Katharina Gaertner,e Cornelia Duscheck,f Ilse Muchitsch,g Christine Marosi,f Michael Schumacher,h Sabine Zzöchbauer-Müller,f Raj K. Manchanda,i Andrea Schrott,j Otto Burghuberk
aMedical University of Vienna, Department of Medicine I, Clinical Division of Oncology and Institute for Homeopathic Research, Vienna, Austria; bHospital of Lienz, Department of Medicine, Lienz, Austria; cGeneral Practitioner, Enns, Austria; dDepartment of Respiratory and Critical Care Medicine, Respiratory Oncology Unit, Karl Landsteiner Institute of Lung Research and Pulmonary Oncology, Klinik Floridsdorf, Vienna, Austria; eInstitute of Complementary Medicine, University of Bern, Inselspital, Bern, Switzerland; fMedical University of Vienna, Department of Medicine I, Clinical Division of Oncology, Vienna, Austria; gAustrian Chamber of Pharmacists, Department Vienna, HomResearch, Interdisciplinary Homeopathic Research Group, Vienna, Austria; hElisabethinenspital, Department of Medicine, Linz, Austria; iCentral Council for Research in Homeopathy, Ministry of AYUSH, Government of India and LMHI, West Delhi, Delhi, India; jStatistikAmbulanz, Consulting Company, Leobendorf, Austria; kDepartment of Respiratory and Critical Care Medicine and Ludwig Boltzmann Institute for Lung Health, Otto Wagner Hospital and Sigmund Freud University, Medical School, Vienna, Austria